5月份中美欧批准上市新药盘点
发布日期:2022-07-04 阅读次数:10604 来源:中国医药报
摘要:
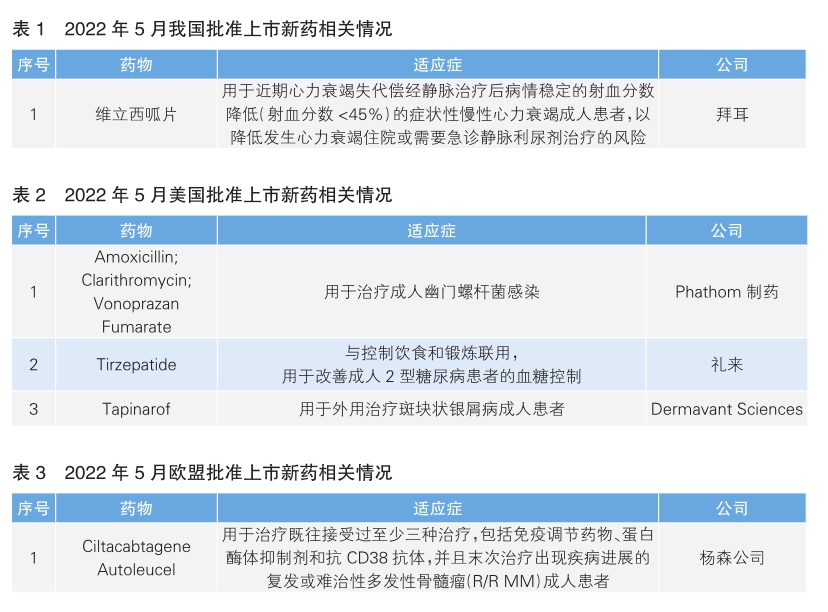
5月份,中美欧共批准5款新药上市。其中,我国批准1款,美国批准3款,欧盟批准1款。
我国批准1款新药上市
5月份,我国批准了1款新药上市,即拜耳公司申报的1类创新药维立西呱片。该药适用于近期心力衰竭失代偿经静脉治疗后病情稳定的射血分数降低(射血分数<45%)的症状性慢性心力衰竭成人患者,以降低发生心力衰竭住院或需要急诊静脉利尿剂治疗的风险。心力衰竭患者死亡风险随入院次数的增加而上升,并随人口老龄化加剧而变得日益普遍。
心力衰竭包括射血分数降低的心衰(HfrEF)和射血分数保留的心衰(HFpEF),前者由心脏不能正常收缩引起,后者由心脏不能正常充盈引起。维立西呱是一种可溶性鸟苷酸环化酶(sGC)刺激剂,通过直接刺激sGC,增加细胞内cGMP(环磷酸鸟苷)的水平,从而松弛平滑肌和扩张血管。该药最早于2021年1月由美国食品药品管理局(FDA)批准上市。
美国批准3款新药上市
根据Pharmadigger数据库数据,5月份美国共批准3款新药上市,均为全球首次批准。
Voquezna Triple Pak(商品名)是Amoxicillin(阿莫西林)、 Clarithromycin(克拉霉素)、Vonoprazan Fumarate(富马酸伏诺拉生)的三重复方组合。其中,伏诺拉生是首款钾离子竞争性酸阻滞剂,也是美国30多年来批准的首款源于新药物类型的创新抑酸疗法。一款新型钾离子竞争性酸阻滞剂(P-CAB),可以竞争性阻滞钾离子与氢/钾离子ATP酶的结合,从而快速抑制胃酸的分泌。伏诺拉生半衰期长,作用时间更持久,因此被视为一种有效的长效质子泵抑制剂(PPI)。此前,FDA已授予伏诺拉生三重以及双重组合疗法合格传染病产品资格(QIDP)和快速通道资格,用于治疗幽门螺杆菌感染。此次FDA的批准是基于一项包含1046名患者的关键性Ⅲ期临床试验的研究结果。试验结果显示,伏诺拉生三重和双重组合疗法达到试验的主要终点,与基于Lansoprazole(兰索拉唑)的三重组合疗法相比,根除率达到非劣效性标准,即在全部患者人群中表现出更优的根除率。
Tirzepatide是首款葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂,GIP和GLP-1是调控血糖的激素,该药可以通过双重作用机制改善血糖控制。患者每周需进行一次皮下注射,可以根据耐受性调节剂量。该药的新药申请被FDA授予优先审评资格。除了帮助2型糖尿病患者控制血糖外,Tirzepatide在治疗未患有2型糖尿病的普通肥胖患者的Ⅲ期临床试验中也获得了积极结果。
Vtama(商品名;Tapinarof,1%)乳膏是芳香烃受体调节剂(TAMA)类药物,可调节淋巴细胞酪氨酸激酶和芳香烃受体活性,抑制银屑病中的炎症性细胞因子产生、炎症细胞的浸润、角质形成细胞的异常角色化增生和血管形成与增生等病理变化。这是美国近25年来获批的首款治疗银屑病的外用新分子实体,代表了一种非类固醇的创新外用治疗类型,其皮肤渗透性良好。尽管Tapinarof分子与此前2019年在我国上市的Benvitimod(本维莫德)乳膏为同一分子实体,但就成药而言,Vtama乳膏每日使用一次,本维莫德每日需使用两次。另外,由于制剂配方、临床试验设计和临床试验结果存在差异,因此这两款药物的直接转化使用需要谨慎。
欧盟批准1款新药上市
5月份,欧盟批准1款新药上市,该药非全球首次批准。
Ciltacabtagene Autoleucel(西达基奥仑赛)是一款具有两种靶向B细胞成熟抗原(BCMA)单域抗体的嵌合抗原受体(CAR)T细胞免疫疗法。2月28日,FDA首次批准该药上市。














