督促医疗器械临床试验持续合规
发布日期:2022-08-04 阅读次数:11933 来源:中国医药报
摘要:
医疗器械临床试验是指在符合条件的医疗器械临床试验机构中,对拟申请注册的医疗器械(含体外诊断试剂)在正常使用条件下的安全性和有效性进行确认的过程。新修订《医疗器械监督管理条例》和《医疗器械注册与备案管理办法》明确,省、自治区、直辖市药品监督管理部门根据医疗器械临床试验机构备案情况,组织对本行政区域内已经备案的临床试验机构开展备案后监督检查,以及对医疗器械临床试验机构遵守医疗器械临床试验质量管理规范的情况进行日常监督检查,监督其持续符合规定要求;并且可以对临床试验的真实性、准确性、完整性、规范性和可追溯性进行现场检查。
广东省药监局在临床试验机构和项目监督管理过程中逐步摸索积累经验,建立了常态化监管工作机制,进一步明确和规范了省内医疗器械临床试验监管的工作程序及检查标准。
试验机构和项目逐年增加
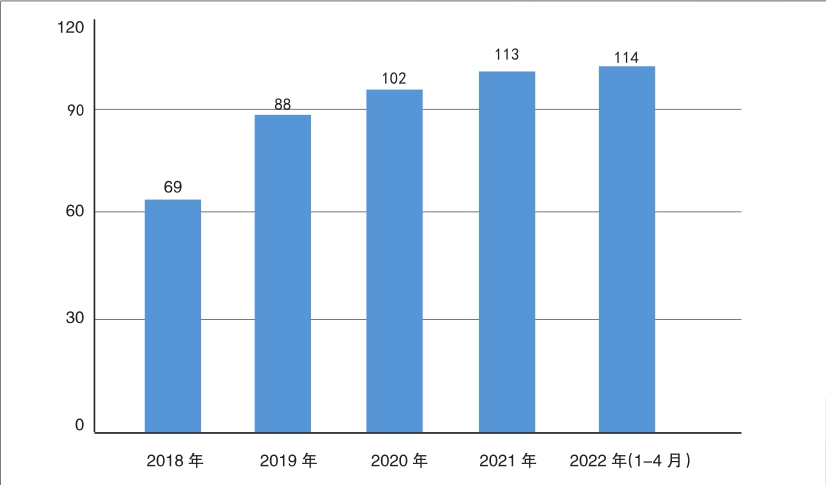
截至今年4月,广东省共有114家医疗器械临床试验机构在国家药监局医疗器械临床试验机构备案管理信息系统中完成备案,数量居全国前列。分年度看,2018年,即《医疗器械临床试验机构条件和备案管理办法》施行的第一年,广东省医疗器械临床试验机构备案数量最多,达到69家,之后新增备案数逐年递减,在2022年到达平台期(详见图)。从地区看,广东省备案医疗器械临床试验机构主要分布在珠三角区域,其中广州44家,占38.6%;深圳31家,占27.2%;佛山、东莞分别有10家、5家。上述4市备案医疗器械临床试验机构数量约占全省的80%。
2017年以来,广东省医疗器械临床试验项目备案维持高位增长,年平均新增备案项目接近400个。从产品类型看,体外诊断试剂临床试验项目年平均新增备案约260个,其他医疗器械临床试验项目年平均新增备案约140个;从管理类别看,第二、三类医疗器械临床试验项目年平均新增备案大致相等,约200个。
积极探索创新监管方式
2017年以来,广东省药监部门积极探索医疗器械临床试验监管方式,通过运用“互联网+”、加强宣传、强化行业自律等措施,取得了显著成效。
运用“互联网+”,医疗器械临床试验备案全程网办 2017年下半年起,广东省药监部门通过优化完善全省许可信息系统,实现备案无纸化网上办理,申办者足不出户即可在业务受理当天完成备案或备案变更,缩减了往返时间及成本,提高了办事效率;同时,沉淀的格式化大数据也为常态化精准监督抽查奠定了良好基础。通过信息化管理方式,广东省药监部门可以随时根据监管需求,按照备案类型、管理类别、产品类型等要求检索某一时间段的医疗器械临床试验项目,有针对性地开展监督抽查。
加强法规文件宣传,鼓励引导临床试验机构备案 2017年底,《医疗器械临床试验机构条件和备案管理办法》发布后,广东省药监部门与卫生部门加大对法规文件的宣贯力度,联合发文鼓励省内符合条件的医疗机构积极开展医疗器械临床试验机构备案。
强化行业自律,成立公益性专委会 2019年1月,广东省药监局依托广东省医疗器械管理学会成立医疗器械临床试验专业委员会。专委会以省内各主要临床试验机构管理人员为主体,吸纳部分资深临床医生及医疗器械生产企业代表,倡导法规研讨和学术交流。
落实“四个最严”要求,保障医疗器械临床试验真实规范 2016年起,广东省药监部门按照“由省内到省外,由在审到在研,由项目到机构,由二类到三类”的思路,逐步常态化地开展医疗器械临床试验监督抽查,合理运用检查结果,不断促进提高申办方规范性开展临床试验,强化医疗器械临床试验机构法律责任意识,提升临床试验检查人员业务水平。同时,广东省药监部门不断加大监督抽查力度,检查频次在2019年度达到高值。通过几年的监督抽查,广东省医疗器械临床试验机构检查覆盖率已经达到73%,计划未来2年内实现全覆盖。
引入社会共治,充实医疗器械临床试验检查资源 临床试验监管是新生事物,起步较晚,检查资源相对不足。2019年5月,广东省药监局在医疗器械临床试验专业委员会基础上,组建评估专家团队,探索以政府购买服务的方式委托开展省内医疗器械临床试验交叉检查;2020年底,广东省药监局组织开展省内临床试验机构监督抽查。评估专家团队成员均为广东省各主要临床试验机构的医疗器械临床试验项目管理者,具备良好的专业素质,了解申报产品的技术特点,熟悉医疗器械临床试验项目质量控制管理流程等,成为检查资源的有力补充。
全方位加强临床试验监管
总结广东省医疗器械临床试验管理经验,建议各级监管部门细化职责分工,加强对临床试验机构和项目的监督管理,完善检查结果处理,推进监管能力建设,更好进行临床试验监管。
目前,各省份医疗器械临床试验机构数量已趋于平稳,药品监管部门应该实现全覆盖检查。从风险管控角度讲,既往未获得药物临床试验资质的临床试验机构,从业经验相对不足、质量管控较难保障,监管部门需要及时掌握其医疗器械临床试验实际情况,增强其法规意识。因此,对于备案机构数量较多的省份,建议首先覆盖检查该类机构;对于原已具备药物临床试验资质的机构,可以与药物临床试验机构合并检查,提高检查效率。
医疗器械临床试验项目不仅数量多,而且持续新增,一个项目从备案到实施再到结题,往往要历经数月甚至数年时间。建议以监督抽查的方式,按照每年随机抽取不少于20%的比例对项目开展现场检查,尽量涵盖医疗器械和体外诊断试剂两类产品,优先选取在新机构开展的新项目;对于注册审评审批、严重不良事件及投诉举报信访等涉及的问题线索,开展有因飞行检查。
发现临床试验机构不具备《医疗器械临床试验机构条件和备案管理办法》规定的条件和要求的,应当责令其限期整改并在整改完成后提出复查申请,整改期内不得承接新的医疗器械临床试验项目,复查仍未通过的,取消其备案,并通报同级卫生健康主管部门;项目检查时发现存在真实性问题的,监管部门应在详尽调查事由、公正厘清责任并充分听取申辩的基础上,依据《中华人民共和国行政许可法》《医疗器械监督管理条例》的规定对责任方作出严肃处理。
此外,监管部门还应当建立适应本行政区域医疗器械产业发展实际的职业化专业化医疗器械临床试验检查员队伍,不断加强法规业务培训,提高检查员能力水平。建议以省为单位成立行业自律组织,加强法规宣贯培训,引导强化行业自律。
相关新闻

复星医药:子公司复迈替尼片注册申请受理
6月6日,复星医药公告称,公司控股子公司上海复星医药产业发展有限公司自主研发的复迈替尼片用于治疗2岁及2岁以上儿童1型神经纤维瘤病(NF1)相关的丛状神经纤维瘤(PN)的药品注册申请于近日获国家药监局受理并已被纳入优先审评程序。
16674个小时之前

国家药监局部署加强医疗器械临床试验机构监管
16674个小时之前

在罕见疾病药物临床研发中应用去中心化临床试验的技术指导原则发布
近日,国家药监局药品审评中心(以下简称药审中心)发布《在罕见疾病药物临床研发中应用去中心化临床试验的技术指导原则》(以下简称《指导原则》)。《指导原则》自发布之日起施行。
16719个小时之前

2024年全国药品抽检中期工作会召开
16719个小时之前

全国疫苗监管质量管理体系建设工作交流会召开
16719个小时之前













